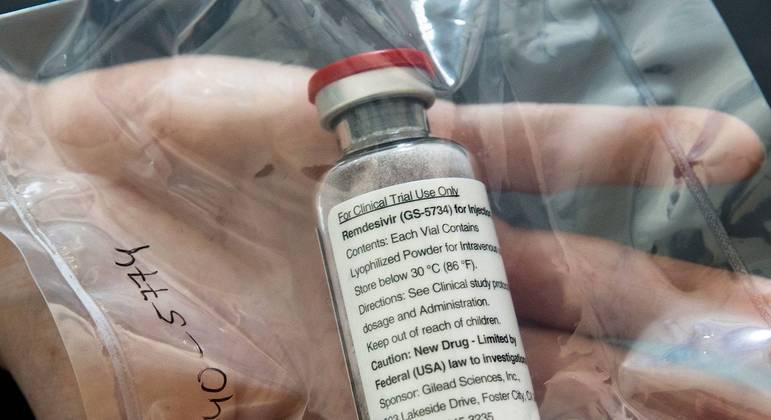
Antiviral Remdesivir é o primeiro medicamento contra a Covid no Brasil Foto: REUTERS
Agência deu o primeiro registro de um medicamento contra a Covid-19; aval permanente é um sinal verde para que o imunizante seja distribuído e utilizado para toda a população prevista na bula. A Anvisa também deu o registro definitivo da AstraZeneca, vacina usada no Brasil desde janeiro e suspensa em alguns países da Europa
A Agência Nacional de Vigilância Sanitária aprovou nesta sexta-feira, 12/03, aprovou o registro do antiviral Rendesivir que terá, em bula, a indicação de uso para tratamento da covid-19. O gerente-geral de Medicamentos e Produtos Biológicos da Anvisa, Gustavo Mendes, informou também que a Anvisa concedeu o primeiro registro para um medicamento com uso indicado em bula para tratamento da covid-19, o Remdesivir, da farmacêutica Gilead.
O Remdesivir é um medicamento sintético intravenoso – aplicado na veia do paciente – que age supostamente impedindo a replicação viral. A Anvisa recomendou o uso para adultos e adolescentes com idade igual ou superior a 12 anos e com peso corporal de, pelo menos, 40 kg, com pneumonia e que requerem administração suplementar de oxigênio de baixo ou alto fluxo, ou outra ventilação não invasiva (que não estão intubados), no início do tratamento.
Além disso, a Anvisa também aprovou o registro definitivo à vacina contra covid-19 desenvolvida pela Universidade de Oxford e a farmacêutica AstraZeneca, com uma etapa de fabricação no Brasil pela Fiocruz (Fundação Oswaldo Cruz).
A vacina Oxford/AstraZeneca já tinha registro para uso emergencial, aprovado por unanimidade em janeiro deste ano pela Anvisa.
A vacina da Pfizer foi a primeira a receber registro definitivo da Anvisa em fevereiro deste ano. O processo levou 17 dias de análise até as doses serem liberadas. Segundo pesquisas, a vacina tem 95% de eficácia contra o coronavírus.
Publicidade
continuação da matéria…
Desenvolvimento de vacinas
Para ser aprovada, a vacina precisa passar por estágios de desenvolvimento. O estágio inicial é feio em laboratório, com análise do vírus e de moléculas para definição da melhor composição do produto, explica a Anvisa.
Depois, a vacina é testada em animais, que são expostos ao agente causador da doença. Na etapa de estudos clínicos com três fases, são feitos testes em humanos desde que se tenha dados preliminares de segurança e possível eficácia.
Para liberar o registro do imunizante, técnicos especializados da Anvisa revisam todos os documentos para validar a segurança da vacina.
Publicidade
continuação da matéria…
Três países europeus suspenderam o uso da vacina Oxford/AstraZeneca
Romênia, Tailândia e Bulgária se juntaram a outros países como Dinamarca e Finlândia na suspensão da vacinação com as doses de AstraZeneca/Oxford depois que algumas pessoas que receberam essas doses desenvolveram coágulos sanguíneos.
A Agência Europeia de Medicamentos está investigando a relação entre as vacinas e esses efeitos. Entretanto, salientou que ainda não havia nenhuma comprovação de ligação entre os casos de trombose e a vacina e que a suspensão temporária era somente uma precaução.
Nesta quinta, o Governo dinamarquês decidiu adiar o uso da vacina por duas semanas, depois que uma mulher de 60 anos sofreu um trombo e morreu, conforme confirmado pelas autoridades do país.